von Dr. Merle C. Hönig
Der positive Einfluss des Lebensstils

Wissen Sie, was Ronald Reagan, Etta James und Rudi Assauer gemeinsam hatten, außer, dass sie Persönlichkeiten des öffentlichen Lebens waren? Die Antwort auf diese Frage lautet: Alle drei erhielten im Laufe ihres Lebens die erschütternde Diagnose Alzheimer, die mit einem unaufhaltsamen Gedächtnisverlust einhergeht, der durch die Ablagerung von schädlichen Eiweißen im Gehirn bedingt ist. Aber obwohl alle drei dieselben Symptome zeigten, unterschieden sie sich im zeitlichen Verlauf der Erkrankung und besonders hinsichtlich des Alters, als sie die verheerende Diagnose erhielten. Ronald Reagan erhielt mit 83 Jahren die Diagnose und verstarb mit 93 Jahren. Bei Etta James wurde die Erkrankung im Alter von 71 Jahren festgestellt. Sie verstarb nur zwei Jahre später. Rudi Assauer hingegen erhielt mit 63 Jahren die Diagnose und verstarb 10 Jahre später. Diese Beispiele stellen nur einen minimalen Bruchteil von etwa 55 Millionen Menschen dar, die derzeit von dieser Erkrankung weltweit betroffen sind. Dennoch veranschaulichen sie, dass die Alzheimer Erkrankung zwar durch charakteristische Symptome, wie zum Beispiel den Gedächtnisverlust, geprägt ist, aber dass das Alter zum Zeitpunkt der Diagnose sowie der Verlauf der Erkrankung von Patient zu Patient unterschiedlich sein können. Ein besseres Verständnis über mögliche Faktoren, die diese Unterschiede begründen, ist zum einen für die frühzeitige Diagnose und die Vorhersage des Krankheitsverlaufes, als auch für die Entwicklung von neuen therapeutischen Ansätzen wichtig. In den letzten Jahren hat deshalb der mögliche positive Einfluss des Lebensstils (z.B. Bildung, Schlaf, Rauchen, Sport) vermehrtes Interesse in der Alzheimer Forschung gewonnen.
Aus vielen Untersuchungen ist bekannt, dass besonders Bildung eine gesundheitsförderliche Lebensweise unterstützen kann. In der Nuklearmedizin der Uniklinik Köln und dem Institut für Neurowissenschaften und Medizin II wollten wir daher herausfinden, ob bestimmte Lebensstilfaktoren wie Bildung oder Schlaf den Zeitpunkt der ersten Symptome der Alzheimer Erkrankung hinauszögert, und mit einer Schwächung des schädlichen Einflusses der alzheimer-typischen Eiweiße zusammenhängt. Zeitgleich wollten wir einen Mechanismus identifizieren, der zur Ausbreitung dieser schädlichen Eiweiße beiträgt. Um diese Forschung besser zu verstehen, ist es sinnvoll, zunächst kurz die schädlichen Eiweiße der Alzheimer Erkrankung sowie die wichtigste nuklearmedizinische Untersuchungsmethode, nämlich die Positronen-Emissions-Tomographie (in kurz PET), zu erklären.
Die aussagekräftigste Bildgebung zur Diagnose der Alzheimer Erkrankung – Die Positronen- Emissions-Tomographie
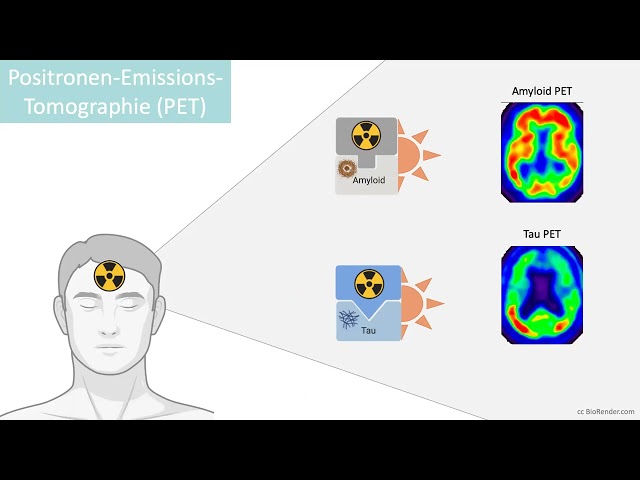
Die Alzheimer Erkrankung ist durch zwei Eiweiße im Gehirn charakterisiert: Die sogenannten Amyloid- und Tau-Eiweiße. Amyloid sammelt sich außerhalb der Nervenzellen (Neurone) im Gehirn an. Tau hingegen häuft sich im Neuron an. Mittels der PET-Bildgebung können wir heutzutage die Ansammlung dieser Eiweiße im lebenden Patienten untersuchen. Dafür werden spezielle radioaktive Substanzen in die Armvene des Patienten gespritzt, die in das Gehirn gelangen und sich dort mit den jeweiligen Eiweißen verbinden. Das Ganze funktioniert wie ein Schlüssel-Schloss-Prinzip. Jede radioaktive Substanz stellt einen einzigartigen Schlüssel dar, der nur in ein bestimmtes Schloss passt, zum Beispiel ein bestimmtes Eiweiß (Amyloid oder Tau). Dort, wo eine Verbindung entsteht, also der Schlüssel ins Schloss passt, werden Strahlen abgesondert, die wir mit der PET-Maschine sichtbar machen können. Die Stärke der Strahlung gibt uns dann Hinweise darüber, wo im Gehirn sich die Eiweiße ablagern und wie viele Eiweiße sich bereits an einer bestimmten Stelle im Gehirn abgelagert haben. Je mehr Ablagerungen sich an einer Stelle im Gehirn befinden, desto stärker strahlt das Signal.
2002 haben zwei amerikanische Wissenschaftler einen Schlüssel entwickelt, mittels dessen man das Amyloid (Schloss) im Gehirn eines lebenden Patienten betrachten kann. Für die Tau-Eiweiße hingegen stand bis vor Kurzem keine spezifische Substanz zur Verfügung, da der passende Schlüssel noch nicht gefunden war. Erst 2015 wurde die Alzheimer Forschung durch die Einführung von radioaktiven Tau-Substanzen (Schlüssel) revolutioniert. Internationale Forschergruppen wendeten diese Technik in großen Gruppen von Alzheimer Patienten an und fanden heraus, dass sich Tau in einem typischen Muster über das Gehirn ausbreitet und enger mit dem Absterben der Neurone und den Symptomen zusammenhängt als Amyloid.
Wie breitet sich die Erkrankung aus und warum unterscheiden sich Alzheimer Patienten:innen in der Schwere der Erkrankung?
Auch am Forschungszentrum Jülich verwenden wir diese neue Technik, die nur wenigen Instituten in Deutschland zur Verfügung steht. Aufgrund der Neuheit der Tau-PET-Bildgebung untersuchten wir zunächst einen möglichen Mechanismus, der zur Ausbreitung von Tau beiträgt, nämlich die sogenannte funktionelle Konnektivität. Die funktionelle Konnektivität kann als Kommunikationsmechanismus zwischen den Hirnarealen verstanden werden. Wenn mehrere Areale gleichzeitig aktiv sind, dann sind sie funktionell miteinander verbunden und werden als ein Netzwerk bezeichnet. Wir fanden heraus, dass die funktionelle Konnektivität, also die Kommunikation zwischen den Gehirnarealen, mit der Verteilung von Tau in Zusammenhang steht. Wir und andere Gruppen zeigten, dass je stärker Gehirnareale innerhalb eines Netzwerks miteinander kommunizieren, desto wahrscheinlicher ist es, dass sich Tau-Eiweiße entlang dieser Netzwerke ausbreiten. Der Befall dieser Netzwerke bewirkt deren Fehlfunktion, welche schlussendlich zum Auftreten der alzheimer-typischen Symptome führt, wie beispielsweise der Verlust von wertvollen Erinnerungen und schließlich auch der Persönlichkeit.
Dieser Ausbreitungsmechanismus trug höchstwahrscheinlich dazu bei, dass Ronald Reagan, Etta James und Rudi Assauer an denselben verhängnisvollen Symptomen litten. Er kann aber nicht erklären, warum sich ihre Krankheitsverläufe unterschieden. An dieser Stelle kommen wir nun zu den möglichen Einflüssen des Bildungsstatus und Lebensstils. Im Rahmen dieses Textes können wir nicht auf die biografischen Details der drei Persönlichkeiten eingehen. Kurzgefasst: Alle drei wiesen unterschiedliche Lebensstile und Bildungsniveaus auf. Genau hier setzen unsere weiteren Untersuchungen an. In einer Gruppe von Alzheimer-Patienten erforschten wir den Einfluss von Bildung auf die Verteilung der Tau-Eiweiße. Wir fanden heraus, dass Alzheimer-Patienten mit einem höheren Bildungsniveau mehr Tau-Eiweiße tolerieren können als Patienten mit einem geringeren Bildungsniveau aber gleichem Ausmaß an kognitiven Einbußen. Insbesondere beobachteten wir, dass höher gebildete Patienten schädliche Tau-Eiweiße in Hirnarealen aufwiesen, die normalerweise erst zum Ende der Erkrankung betroffen sind. Dennoch waren die alzheimer-typischen Symptome bei diesen Patienten nur leicht ausgeprägt.
„Bildung ist die mächtigste Waffe der Welt“ sagte niemand anderes als Nelson Mandela. Ist Bildung auch eine Waffe gegen die Alzheimer Erkrankung?
Diese Beobachtung ließ uns die Hypothese aufstellen, dass ein höheres Maß an Bildung Abwehrmechanismen gegen die Alzheimer-Erkrankung fördert. Wir vermuten, dass ein noch nicht näher bekannter Abwehrmechanismus den schädlichen Einfluss der Tau-Eiweiße mildert. Dies würde bedeuten, dass Neurone trotz der eingelagerten Tau-Eiweiße über einen längeren Zeitraum funktionsfähig bleiben und nicht direkt absterben. Wir gingen dieser Frage nach, indem wir den Zuckerverbrauch im Gehirn von Alzheimer-Patienten mittels der PET-Technik untersuchten. Der Zuckerverbrauch ist ein Maß für die Lebendigkeit unserer Neurone. Tatsächlich konnten wir zeigen, dass bei höher gebildeten Patienten die Einlagerung der Tau-Eiweiße weniger stark mit einer Verminderung der Funktionsfähigkeit der Neurone zusammenhängt. Das bedeutet, dass die Neurone bei Patienten mit einem höheren Bildungsniveau, trotz weit verbreiteter Tau-Eiweiße, relativ funktionsfähig bleiben. Aufgrund der nur leicht eingeschränkten Lebendigkeit der Neurone zeigen höher gebildete Patienten wahrscheinlich daher nur leichte kognitive Einbußen zum Zeitpunkt der Diagnose.
In unseren Arbeiten haben wir zwar noch nicht die direkten Schutzmechanismen gegen den schädlichen Einfluss der Tau-Eiweiße entdeckt, aber unsere Forschungsergebnisse belegen, dass ein Faktor des frühen Lebensalters, nämlich Bildung, eng verbunden mit dem Auftreten und dem Ausmaß der Alzheimer-Erkrankung ist.
Kann ich auch im Schlaf gegen die Erkrankung vorbeugen?
In einem neuen Projekt wollen wir nun herausfinden, ob die Schlafqualität einen Einfluss auf das Entstehen und das Fortschreiten der Alzheimer Erkrankung hat. Eine neue Vermutung ist, dass im gesunden Gehirn diese Eiweiße im Schlaf aus dem zentralen Nervensystem gewaschen werden. Schlaf ist quasi eine Spülmaschine des Gehirns. Bei der Alzheimer-Krankheit ist dieser Reinigungsprozess wahrscheinlich gestört. Die Proteine verklumpen zu schädlichen Ablagerungen und Nervenzellen sterben ab. Anhaltende Schlafstörungen sind deshalb ein Risikofaktor für die Alzheimer-Krankheit. Besonders die Länge des Tiefschlafs scheint dabei entscheidend zu sein. In dem neuen Projekt untersuchen wir, ob die Länge des Tiefschlafs eine Vorhersagekraft für den Verlauf der Alzheimer Krankheit hat. Darüber hinaus wollen wir herausfinden, ob Personen, die eine hohe Schlafqualität aufweisen, ein geringeres Risiko für die Alzheimer Erkrankung tragen und weniger alzheimer-typische Proteine aufzeigen. Falls das so ist, dann könnte die Behandlung von Schlafstörungen einen Ansatz gegen die Alzheimer Erkrankung bieten.
Auch wenn bisher die genauen Schutzmechanismen gegen die Alzheimer Erkrankung noch nicht gefunden wurden, stellen Lebensstilfaktoren ein wichtigen Ansatz dar, da wir diese selbst beeinflussen können. Sie bieten damit einen möglichen therapeutischen Ansatz für die Alzheimer-Erkrankung, für die es bisher immer noch keine effektive Behandlungsmethode gibt. In Anbetracht unserer zunehmend alternden Bevölkerung ist die weitere Erforschung von schützenden Faktoren, die durch einen gesunden Lebensstil unterstützt werden, essentiell für die Entwicklung von neuen Behandlungsmethoden, die hoffentlich eines Tages das Leid von Millionen Patienten und deren Angehörigen lindern können. Zudem können diese Lebensstilfaktoren generell zum gesunden Altern beitragen, ohne dass man an dieser heimtückischen Erkrankung des Alterns leidet.
Falls Sie Interesse an unseren aktuellen Studien haben, melden Sie sich gerne unter studien-mmni@uk-koeln.de.
Wir freuen uns, von Ihnen zu hören.
Alzheimer - Was ist denn eigentlich gesund?
von Dr. Nora Bittner

Sprechen wir über die Alzheimer-Erkrankung, dann ergibt sich automatisch auch die Frage: Was ist denn (noch) gesund? Dieser Fragestellung widmen wir uns in der großangelegten 1000-Gehirne-Studie, die von 2011 bis 2018 am Forschungszentrum in Jülich durchgeführt wurde. Um tiefgreifende Erkenntnisse zu sammeln, wie die „normale“ Alterung des Gehirns sich äußert, unterzogen sich 1314 Probanden/innen einer Kernspin-Tomographie des Gehirns. Mittels dieser Technik ist es möglich die Gehirnstruktur eines lebenden Menschen zu rekonstruieren, sowie die funktionelle Konnektivität zu untersuchen – also den oben angesprochenen Kommunikationsmechanismus zwischen den Hirnarealen. Zusätzlich sammelten wir viele weitere Informationen u.A. zum Bildungsstand, Vorerkrankungen und dem Lebensstil und testeten motorische und kognitive Fähigkeiten. Alle Probanden/innen stammen dabei aus einer Kohorte, der Heinz-Nixdorf-Recall und Mehr-Generationen-Studie, die populations-basiert ausgerichtet ist. Dies bedeutet, dass die Teilnehmer/innen zufällig aus dem Bürgerregister der Ruhr-Region gewählten wurden.
Alterung ist sehr variabel
Noch einmal zurück zu Ronald Reagan, Etta James und Rudi Assauer: Wir stellten bereits fest, dass sich ihre Krankheitsverläufe unterschieden, obwohl sie unter derselben Erkrankung litten. Unter den Probanden/innen der 1000-Gehirne-Studie sind sehr wenige Personen, die Anzeichen von Demenz zeigen. Aber auch innerhalb dieser Personen, die „normal“ altern, beobachten wir, dass die kognitiven Fähigkeiten sehr variabel sind: Eine Person kann mit 80 Jahren kognitiv jung und „fit“ sein, während eine andere Person gleichen Alters kognitive Beeinträchtigung wie z.B. Gedächtniseinschränkungen erlebt. Wir nehmen an, dass diese kognitiven Unterschiede auf Unterschieden in der Gehirnstruktur und der -funktion beruhen. Im Allgemeinen stellen wir dabei fest, dass das Gehirn mit höherem Alter an Volumen verliert. Dies betrifft unterschiedliche Regionen unterschiedlich stark, sodass einige kognitive Fähigkeiten eher abbauen (z.B. das Gedächtnis) als andere (z.B. sprachliche Fähigkeiten). Doch wie erklären sich nun die Unterschiede in der Gehirnstruktur und der -funktion? Auch hier gelangen wir wieder zu den möglichen Einflüssen des Bildungsstatus und Lebensstils.
Bildung und „normale“ Alterung
Wir stellten bereits die Hypothese auf, dass ein höheres Maß an Bildung Abwehrmechanismen gegen die Alzheimer-Erkrankung fördert. Könnte Bildung also auch ein Einflussfaktor sein, der (unter anderem) fördert, dass wir gesund oder normal altern? Mit einer höheren Bildung scheint allgemein eine höhere kognitive Leistungsfähigkeit einherzugehen und auch ein größeres Gehirnvolumen. Oben erfuhren wir bereits, dass das Gehirnvolumen mit zunehmendem Alter tendenziell abnimmt. Daraus ergibt sich die Annahme, dass diejenigen Personen mit einer höheren Bildung die Grenze, ab der die Abnahmen im Volumen zu einer kognitiven Beeinträchtigung führen, erst später erreichen und so länger geschützt sind – hier sprechen wir davon, dass diese Personen eine höhere „Reserve“ aufweisen. Eine weitere Fähigkeit, die mit einer höheren Bildung einhergeht und somit auch im „Verdacht“ steht zu dieser Reserve zusätzlich beizutragen, ist Mehrsprachigkeit. Auch hier wird angenommen, dass das Erlernen einer zweiten (oder mehrerer) Sprache(n) eine kognitive Herausforderung darstellt, die uns im Alter vor Abbau-Prozessen schützt.
Was macht der Lebensstil?
Die weitere Forschung der 1000-Gehirne-Studie möchte Faktoren identifizieren, die über die Bildung hinaus erklären, weshalb manche von uns früher altern, als andere. Im besonderen Fokus steht dabei der Lebensstil, den wir Menschen selber beeinflussen können. In einer Studie entwickelten wir daher eine Methode ein gesammeltes Lebensstil-Risiko zu messen: Das kann man sich so vorstellen, dass eine Person, die viel raucht und Alkohol konsumiert und dabei wenig körperlich und sozial engagiert ist, möglicherweise ein höheres Risiko aufweist, dass das Gehirn schneller altert, als eine Person, die raucht und Alkohol konsumiert, aber dennoch körperlich und sozial sehr aktiv ist. Hierbei stellte sich heraus, dass einer der entscheidenden Faktoren für den stärkeren Erhalt der Gehirnstruktur die körperliche Aktivität ist, kombiniert mit höherer sozialer Aktivität und niedrigem Alkoholkonsum, Vermehrtes Rauchen führt im Gegensatz eher dazu, dass die funktionelle Konnektivität (die Kommunikation zwischen Gehirnarealen) anders ausgeprägt ist. Dies könnte daraufhin deuten, dass kognitive Prozesse bei Rauchern anders ablaufen und dadurch Strategien um den altersbedingten Verlust an Gehirnvolumen aufzufangen weniger effizient sind.
Mehr dazu: Pressemeldung "Lebensstil hinterlässt Spuren im Gehirn"
Lässt sich vorhersagen, wer schneller oder langsamer altert ?
Weiterhin gibt es im Bereich der „normalen“ Alterungsforschung Bemühungen vorherzusagen, ob bei älteren Personen, die bisher nicht dementiell erkrankt sind, ein Risiko für eine Alzheimer-Erkrankung besteht oder eine beschleunigte Alterung vorliegt. In Zusammenarbeit mit der Universität in Jena nutzten wir daher die Aufnahmen der Gehirnstruktur der Probanden/innen und trainierten eine künstliche Intelligenz, sodass diese erlernte auf Grund der Aufnahmen zu schätzen, wie alt die Person ist. Das geschätzte Alter wich dabei im Durchschnitt ca. 3,9 Jahre vom „wahren“ chronologischen Alter ab. Es gibt also Menschen, deren Gehirne jünger aussehen, als sie tatsächlich sind. Doch welche Eigenschaften zeichnen diese Menschen aus? Auch hier untersuchten wir wieder den Lebensstil. Allgemein ging ein niedrigeres Gesamt-Lebensstil-Risiko mit einem jünger ausschauenden Gehirn einher: Als besonders günstiger Einflussfaktor trat wieder vermehrte körperliche Aktivität hervor. Zusätzlich stellten wir fest, dass das Gehirn-Alter von Personen, die rauchen, tendenziell älter geschätzt wird: Bei starken Rauchern/innen wurde das Gehirnalter im Durchschnitt 4.9 Jahre älter geschätzt als bei denjenigen, die niemals geraucht haben. Frühere Studien (Karama et al., 2015) zeigten allerdings auch, dass diese Unterschiede zwischen Rauchern/innen und Nicht-Raucher/innen wieder geringer werden, nachdem mit dem Rauchen aufgehört wird – ein ermutigendes Ergebnis!
Können wir uns gesund schlafen?
Wie oben bereits erwähnt, ist auch guter Schlaf in den Fokus für eine langanhaltende Gesundheit gerückt. Insbesondere kann dies relevant werden, wenn unser Schlafverhalten unserem Schlafbedürfnis widerspricht: D.h. wenn wir weniger gut, lang oder tief schlafen, als wir eigentlich benötigen. Die aktuelle Forschung geht dabei davon aus, dass jeder Mensch individuelle Schlafpräferenzen hat - Manche von uns sind „Lerchen“ und sehr früh wach, die große Mehrheit wird zu den üblichen Morgenzeiten aktiv und einige sind richtige „Nachteulen“, die spätabends weitaus leistungsfähiger sind als früh morgens. Man nimmt an, dass dies gesundheitlich relevant werden kann, wenn unser Bedürfnis unserem Verhalten widerspricht, z.B. bei Nacht-Schichtarbeit. In einer Studie untersuchten wir daher, ob Schichtarbeit ebenfalls ein Faktor ist, der für die normale Alterung des Gehirns relevant sein könnte. Wir untersuchten hierbei ebenfalls die Gehirnstruktur, die funktionelle Kommunikation innerhalb großer Gehirnnetzwerke, sowie die kognitive Leistungsfähigkeit. Wir fanden hierbei nur sehr geringe Hinweise darauf, dass Schichtarbeiter/innen im Vergleich zu Nicht-Schichtarbeiter/innen Unterschiede im Gehirn aufweisen. Möglicherweise ist es daher weniger ausschlaggebend ob jemand Schichtarbeit macht oder nicht, sondern wichtiger, ob dennoch ein gesunder Schlaf möglich ist.
Zusammengenommen ist es essentiell schützende Faktoren weiter zu erforschen um so einerseits einen gesunden Lebensstil zu fördern und so auch eine möglichst „gesunde Alterung“ zu begünstigen, sodass das Risiko eine Alzheimer-Erkrankung zu entwickeln verringert wird, und andererseits um Behandlungsmöglichkeiten und frühzeitige Interventionen zu entwickeln, die im Falle einer Erkrankung die Symptome abzumildern.